Problemas preparación primer parcial Ampliación de Genética

Si estudias Biología en la Universidad de Alicante (la UA para los amigos), en tercero tienes uno de los huesos más duros de roer de la carrera. Si no tuviste suficiente en primero con Genética… ¡¡ahora tienes Ampliación de Genética!!
Los profesores de la UA han dado dos problemas para que te prepares el primer parcial. Aquí los tienes resueltos por nuestros profesores. Estos dos problemas, junto a todos los de la serie, las explicaciones de los temas y la resolución de los test la tienes en nuestro Campus.
Para saber la info de nuestro curso de Ampliación de Genética y de otras asignaturas de tu carrera pulsa este enlace.
¡Demos la bienvenida a tus nuevos amigos: Brenda, John & Mary!
Problema 1. Brenda
Este problema se centra en la herencia recesiva ligada al cromosoma X de DMD, evaluando el uso de marcadores moleculares D2 y L128 para predecir el riesgo en la descendencia. Importante tener en cuenta la recombinación, los pasos de una PCR y tener claro los tipos de marcadores y como funcionan.
[VID-34802] Problema 1: Distrofia Muscular de Duchenne (DMD) (37:01)
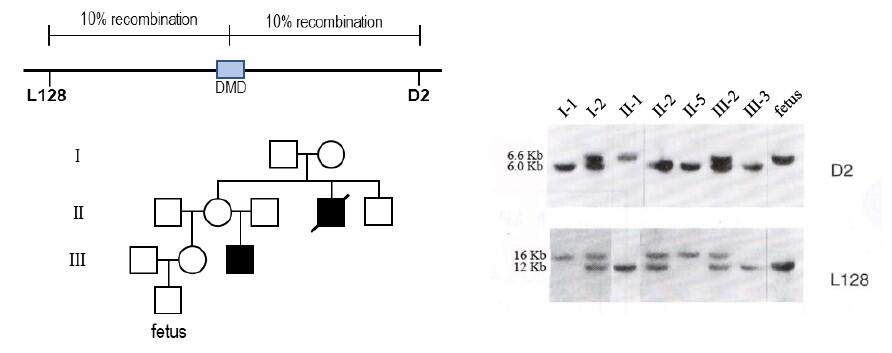
Al revisar antiguos archivos de diagnóstico genético, encontramos los datos de esta familia. Brenda (III-2) tenía un hermanastro que padecía distrofia muscular de Duchenne y un tío fallecido que también la padecía. Nadie más en la familia estaba afectado por la enfermedad. Ella decidió hacerse una prueba genética para saber si el hijo que estaba esperando estaría afectado. Había disponibles dos marcadores moleculares, D2 y L128, ambos ubicados en el cromosoma X y muy cerca del gen DMD, cuyas mutaciones causan la enfermedad (ver figura).
Usa la siguiente nomenclatura: D para los alelos WT (tipo silvestre) y d para los alelos mutantes del gen DMD, y números para los alelos de los marcadores.
Indica:
- Los individuos en el árbol genealógico que sin duda tienen que ser portadores.
- Basándote en la información proporcionada en la figura, ¿qué tipo de marcadores son D2 y L128?
- La técnica de análisis utilizada para obtener los resultados de la figura. Haz un esquema de la región genómica para D2 y L128, incluyendo las características relevantes (sitios de unión de cebadores y/o sondas, sitios de restricción, …) para el análisis.
- El genotipo esperado para los siguientes individuos, indicando con una barra la fase de ligamiento para el gen de la enfermedad y los marcadores asociados. Justifica tu respuesta.
- I-2
- II-2
- La probabilidad de que el bebé de Brenda esté sano.
- ¿Son informativos los marcadores utilizados? Justifica tu respuesta.
Unos años después, el gen DMD fue completamente secuenciado y descrito como el gen más grande hasta ese momento en el genoma humano: más de 2 MB de longitud y 79 exones. La mayoría de las mutaciones identificadas eran deleciones de una o más partes codificantes del gen, que podían detectarse mediante análisis de Southern-blot con una sonda específica. Para entonces, Brenda estaba embarazada nuevamente y se sometió a este nuevo análisis. Carriles: 1- Brenda; 2- Hermanastro de Brenda; 3- Hijo de Brenda; 4- Niño esperado.
- Da una breve explicación de la detección de más de una banda en el Southern-blot.
- Basándote en tu respuesta anterior, la sonda utilizada en el Southern-blot sería (encierra la(s) respuesta(s) compatible(s)):
- cDNA
- Secuencia amplificada por PCR de un intrón
- Secuencia amplificada por PCR de un exón
Este nuevo análisis identificó que, en la familia de Brenda, la mutación específica presente en el gen DMD consiste en una deleción en el exón 56, cuya longitud en el alelo WT es de 897 pb.
- ¿Podríamos diseñar un método más rápido y económico para el diagnóstico genético en esta familia? Haz un esquema simple que incluya los elementos clave para el análisis (cebadores, sitios de restricción, …) e indica los resultados que esperarías.
- ¿Podría usarse el nuevo test prenatal diseñado en una familia diferente no relacionada? Justifica tu respuesta.
Pdf. Enunciado
Vídeo
Errata: En el punto 5 se calcula la probabilidad de que esté enfermo, en vez de que esté sano. Hay que restar a 100% lo que sale en el cálculo (P(Enfermo)+P(Sano)=100%, al ser mutuamente excluyentes y las dos únicas posibilidades).
Problema 2. John & Mary
Este problema explora la herencia de un síndrome renal autosómico dominante, utilizando marcadores genéticos cercanos para rastrear el gen afectado en dos familias. Lo importante a tener en cuenta en este problema es el ligamiento del gen, la probabilidad de recombinación, y el diseño de un método de diagnóstico mediante PCR y digestión enzimática.
[VID-34796] Problema 2. Herencia de Síndrome Renal (36:24)
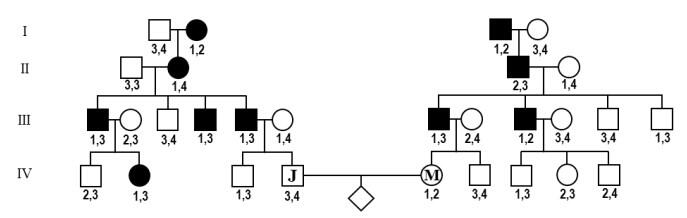
John (IV-4; etiquetado como J) y Mary (IV-5; etiquetada como M) son una pareja de alrededor de 20 años que espera su primer hijo juntos. Ambos pertenecen a familias afectadas por un síndrome renal raro cuyos efectos comienzan a manifestarse a partir de los 30 años. Se sabe que este síndrome es causado por mutaciones puntuales en un gen vinculado a un marcador genético, que se encuentra a 10 cM y puede analizarse fácilmente mediante PCR y electroforesis. Se muestran los árboles genealógicos de ambas familias, donde el genotipo para el marcador genético también está indicado con números debajo de cada individuo.
Usa la nomenclatura adecuada para los alelos del gen de la enfermedad (A/a para dominante/recesivo, respectivamente) y números para los alelos del marcador.
Indica:
- ¿Cuál es el modo de herencia de la enfermedad? (0,5 puntos)
- Basándote en la información proporcionada, ¿qué tipo de marcador genético estamos utilizando? (1 punto)
- El genotipo esperado para los siguientes individuos, indicando con una barra la fase de ligamiento para el gen de la enfermedad y el marcador asociado. Justifica tu respuesta. (1,5 puntos)
- IV-2 (Laura, prima de John)
- III-7 (Peter, padre de Mary)
- III-12 (Paul, el tío menor de Mary)
- La probabilidad de que el bebé de John y Mary esté afectado. (2 puntos)
Varios familiares de Mary decidieron contactar un laboratorio privado de análisis genético y solicitaron la secuenciación del gen objetivo. El análisis identificó que, en la familia de Mary, la mutación específica presente generó un cambio en un aminoácido conservado (clave para la regulación de la actividad de la proteína), lo que también resulta en la desaparición de un sitio de restricción para la enzima EcoRI.
- ¿Podríamos diseñar un método rápido y económico para la detección directa de la mutación en esta familia? Haz un esquema simple que incluya los elementos clave para el análisis (cebadores, sitios de restricción, …) e indica/dibuja los resultados que esperarías. (1,5 puntos)
- Laura (prima de John) ahora espera su primer hijo con su esposo, un hombre sano sin antecedentes familiares de ningún síndrome renal. ¿Podría este nuevo test prenatal diseñado usarse para determinar si el niño no nacido estaría afectado por el síndrome? Justifica tu respuesta. (1,5 puntos)